La coqueluche, causée par la bactérie Bordetella pertussis, est une maladie hautement infectieuse et potentiellement mortelle pour les nourrissons. Malgré la disponibilité de vaccins qui protègent contre l’apparition des symptômes, la transmission bactérienne et l’infection subséquente continuent de se propager à travers le monde. Cependant, une équipe internationale de chercheurs a récemment mené un essai clinique de phase 2 sur un nouveau vaccin nasal contre la coqueluche pour les adultes.
La coqueluche est une infection respiratoire très contagieuse causée par la bactérie Bordetella pertussis. Elle se propage par l’air et se caractérise par des quintes de toux violentes, qui peuvent entraîner des vomissements et une difficulté à respirer. Cette maladie peut être particulièrement dangereuse pour les nourrissons, car elle peut entraîner des complications graves, telles que la pneumonie, la convulsion, l’apnée et même la mort. Bien que les vaccins soient disponibles pour prévenir la maladie, la coqueluche continue de se propager dans certaines parties du monde.
Depuis les années 1990, le vaccin dCaT est principalement utilisé pour lutter contre la coqueluche. Cependant, son effet diminue avec le temps et il ne peut pas empêcher l’infection ou la transmission de la bactérie. Les épidémies de coqueluche continuent donc à se propager malgré les vaccins existants.
Vaccin nasal contre la coqueluche plus sûr et plus efficace
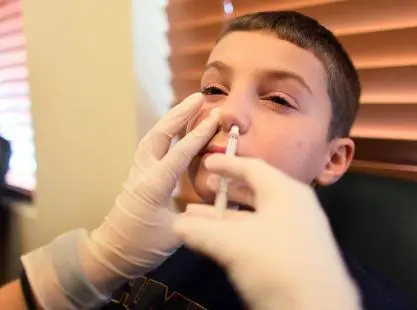
Pour remédier à cela, une nouvelle forme de vaccin appelée BPZE1* a été développée. Elle est administrée par voie nasale et imite les voies de transmission naturelles de la maladie. Une étude de phase 2 menée sur 300 adultes en bonne santé a montré que BPZE1 a induit une immunité plus forte et plus constante au niveau de la muqueuse nasale, empêchant la colonisation bactérienne chez 90 % des participants. De plus, l’infection a régressé plus rapidement chez les personnes vaccinées avec BPZE1 et aucun effet secondaire notable n’a été observé.
Selon Camille Locht, « le profil bénéfice/risque du vaccin BPZE1 est favorable : une seule administration nasale permet d’induire sans danger et avec une bonne tolérance, une immunité forte et durable, tant au niveau sanguin qu’au niveau des voies respiratoires. En outre, contrairement au vaccin dCaT, BPZE1 protège les muqueuses d’une colonisation par la bactérie. »
« Cette bactérie étant hautement infectieuse pour l’être humain, il est critique qu’un vaccin ne cible pas uniquement le développement de la maladie mais également la transmission de la bactérie qui la cause et la vitesse à laquelle l’organisme se débarrasse de cette dernière, ajoute Camille Locht. Dans cette optique, BPZE1 apparaît comme un nouvel outil pertinent pour prévenir les infections de coqueluche et réduire les chaînes de transmission épidémiques. »
* Qu’est-ce que le vaccin BPZE1 ?
En 2008, un groupe de chercheurs a commencé à travailler sur un nouveau vaccin nasal pour la coqueluche. Le vaccin BPZE1 a été développé et breveté par une équipe de l’Inserm et de l’institut Pasteur de Lille dirigée par Camille Locht. En 2014, les chercheurs ont publié les résultats d’un essai clinique de phase 1 montrant l’efficacité et l’innocuité du vaccin BPZE1, après examen par un comité indépendant. Une entreprise nommée ILiAD Biotechnologies a ensuite signé un accord pour poursuivre le développement et l’évaluation du vaccin. En 2020, de nouveaux résultats cliniques ont confirmé la sécurité et l’efficacité du vaccin BPZE1.
Sources :
Immunogenicity and safety of BPZE1, an intranasal live attenuated pertussis vaccine, versus tetanus–diphtheria– acellular pertussis vaccine: a randomised, double-blind, phase 2b trial
Cheryl Keech, MD1, Vicki E. Miller, MD2, Barbara Rizzardi, MD3, Christopher Hoyle, MBA4, Melinda J. Pryor, PhD5, Jonathan Ferrand, PhD5, Ken Solovay, MS1, Marcel Thalen, PhD1,6, Stephanie Noviello, MD1, Peter Goldstein, MS1, Andrew Gorringe, PhD7, Breeze Cavell, PhD7, Qiushui He, MD8, Alex-Mikael Barkoff, MSc8, Keith Rubin, MD1, Camille Locht, PhD9
1 ILiAD Biotechnologies, LLC, Weston, FL USA
2 DM Clinical Research, Texas Center for Drug Development, Houston, TX USA
3 Velocity Clinical Research, West Jordan, UT USA
4 Elite Research Network, Mount Pleasant, SC USA
5 360biolabs, Melbourne Victoria, Australia
6 BioLyo Technologies, BVBA, Ghent, Belgium
7 United Kingdom Health Security Agency, Porton Down, Salisbury UK
8 University of Turku, Institute of Biomedicine, Turku Finland
9 University Lille, CNRS, Inserm, CHU Lille, Institut Pasteur de Lille, U1019-UMR9017–CIIL – Centre for Infection and Immunity of Lille, Lille, France
The Lancet, 10 mars 2023
DOI : https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(22)02644-7/fulltext